
2023年10月17日,中國醫學科學院生物醫學工程研究所梅林團隊與中山大學陳洪中團隊、南洋理工大學趙彥利團隊合作在Nature Communications 《自然通訊》發表了題為“NIR-dye bridged human serum albumin reassemblies for effective photothermal therapy of tumor”(NIR染料橋接人血清白蛋白自組裝納米粒用于腫瘤的高效光熱治療)的論文。該研究開發了一種新型人血清白蛋白(HSA)藥物遞送體系,用于高效負載具有雙馬來酰亞胺結構的近紅外(NIR)染料,實現了抗腫瘤藥物的主動靶向遞送和腫瘤的高效光熱治療。
自白蛋白紫杉醇(Abraxane)在臨床成功應用以來,基于HSA的藥物遞送系統因其具有優異的生物相容性和藥動學性質,已被廣泛應用于腫瘤靶向藥物遞送。盡管目前已經報道了許多基于HSA的藥物遞送系統,這些系統仍然存在藥物負載率低(低于10%)、制備工藝復雜等問題。因此,開發兼具高藥物負載率和高藥物遞送效率的HSA體系制備技術仍然具有挑戰性。在本研究中,該團隊報道了一種新型HSA制劑的制備技術,用于負載具有雙馬來酰亞胺結構的NIR染料BPY(本研究合成的具有光熱活性BODIPY類小分子BPY-Mal2,見圖1)。該制備技術首先通過TCEP[三(2-羧乙基)膦,一種二硫鍵還原劑]將鏈接HSA的二硫鍵剪開,使得HSA失去三級結構變為肽鏈。隨后,再利用馬來酰亞胺和巰基的反應負載BPY,將BPY橋接在肽鏈之間,通過藥物與肽鏈之間的交聯形成自組裝納米粒(圖2)。相比于之前報道的HSA藥物遞送體系,該技術所制備的BPY@HSA顯著提高了藥物負載率(26.1%),并在體外表現出了增強的細胞攝取和3D腫瘤球滲透能力。這是由于改性后的HSA不僅能與gp60結合,還能與gp18和gp30等受體結合,這提高了腫瘤細胞對BPY@HSA的主動攝取效率。體內研究亦表明該體系具有良好的靶向效率,可作為一種新型光熱治療體系用于光熱消融腫瘤。
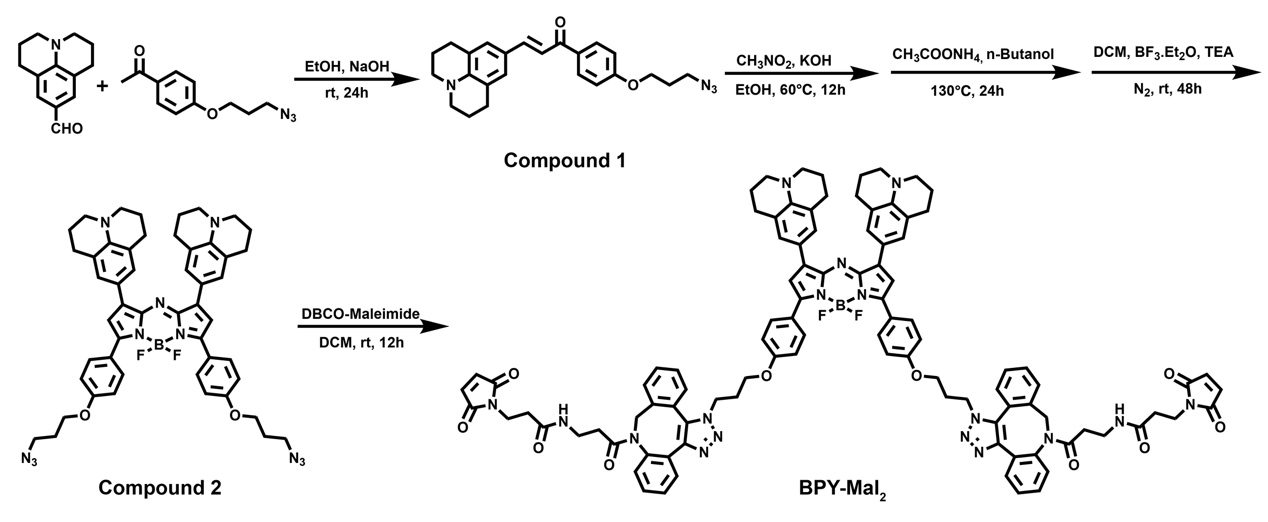
圖1. BPY的合成路線
這項工作開發的HSA藥物遞送系統的藥物負載模式,有望用于實現更多的具有雙馬來酰亞胺結構藥物的高效負載和靶向遞送,以提高藥物遞送效率,將為癌癥和其它疾病的治療藥物的負載提供重要的策略。
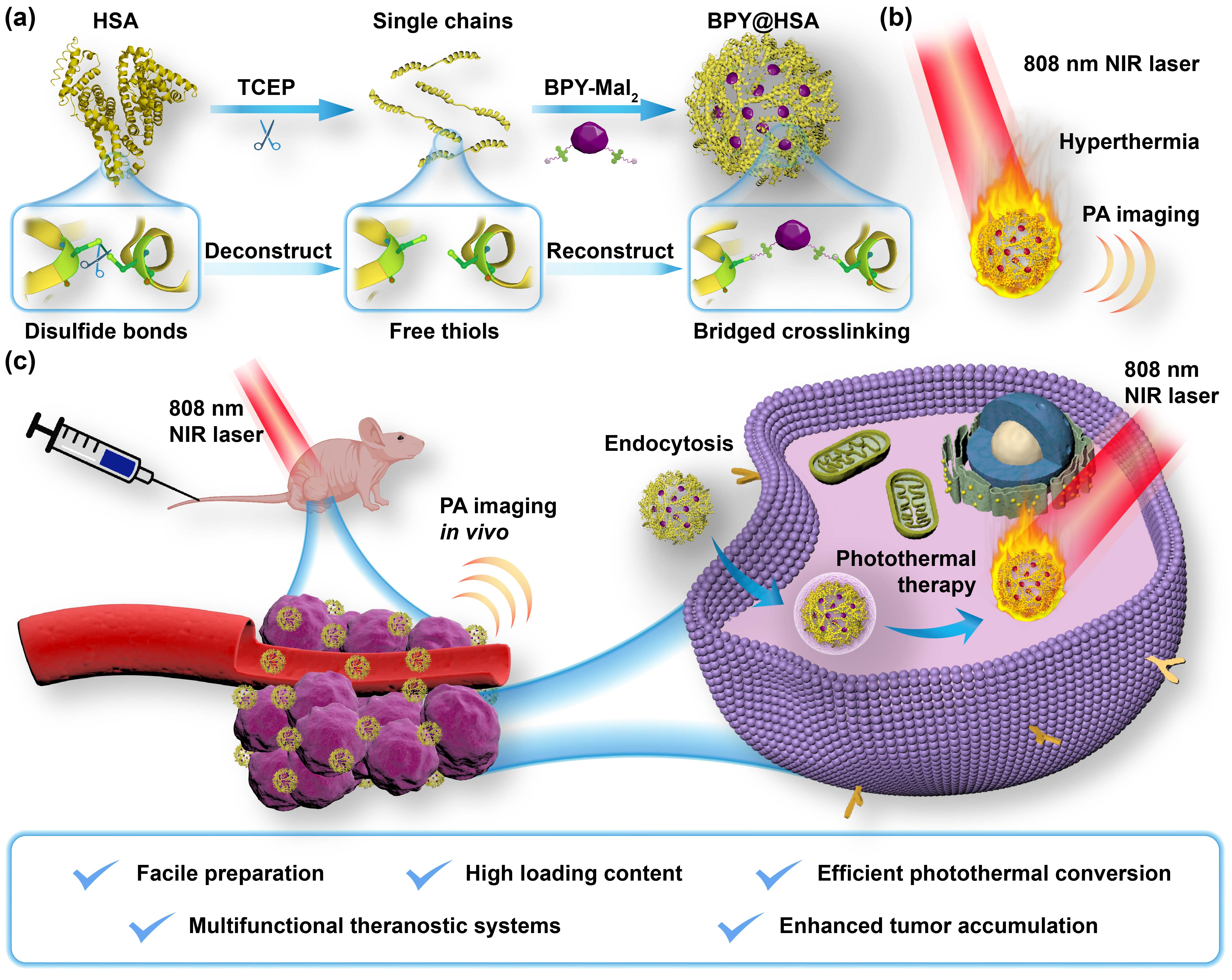
圖2. 開發BPY@HSA用于腫瘤高效光熱治療
本研究工作以中國醫學科學院生物醫學工程研究所為第一作者單位,獲得國家自然科學基金項目(32101065和82272154)、中央高校基本科研業務費(2021-RC310-005)、天津市杰出青年基金(22JCJQJC00120)和中國醫學科學院醫學與健康科技創新工程(2021-I2M-1-058、2022-I2M2-003)等項目資助。中國醫學科學院生物醫學工程研究所和天津市生物醫學材料重點實驗室梅林研究員、新加坡南洋理工大學趙彥利教授和中山大學陳洪中副教授為本文章的共同通訊作者,北京協和醫學院在讀博士生史照青、雒苗苗和中山大學博士生黃啟立為共同第一作者。
論文鏈接:https://www.nature.com/articles/s41467-023-42399-9